第三章 免疫球蛋白与抗体
抗体(antibody,Ab)是B细胞接受抗原刺激后增殖分化为浆细胞所产生的一类能与相应抗原特异性结合的球蛋白。抗体主要存在于血清中,也见于其他体液和外分泌液中,故将抗体介导的免疫称为体液免疫。
在骨髓瘤、巨球蛋白血症等患者血清中也发现了与抗体有相似结构而未证实有抗体活性的球蛋白。在国际免疫学会议上将具有抗体活性或化学结构与抗体相似的球蛋白,统一命名为免疫球蛋白(immunoglobulin,Ig)。免疫球蛋白是化学结构的概念,抗体则是生物学功能的概念;所有的抗体都是免疫球蛋白,而免疫球蛋白不一定都具有抗体活性。
免疫球蛋白可分为分泌型和膜型:前者主要存在于血液及组织液中,具有抗体的各种功能;后者表达于B细胞膜表面,构成B细胞膜上的抗原受体,称为膜型免疫球蛋白(membrane immunoglobulin,mIg)。
第一节 免疫球蛋白的分子结构
一、免疫球蛋白的基本结构
免疫球蛋白的基本结构是由四条肽链通过二硫键连接构成的单体,也是Ig的基本功能单位。其中两条相同的多肽链较长,称为重链(heavy chain,H链)。每条重链约由450~550个氨基酸残基组成,重链间由二硫键相连。另两条相同的多肽链较短,称为轻链(light chain,L链)。每条轻链约含214个氨基酸残基,以二硫键与重链相连。
重链和轻链靠近N端(氨基端)的约110个氨基酸(L链½和H链的¼或⅕处)的组成和排列顺序随抗体特异性的不同变化较大,称为可变区(variable region,V区),用V_H和V_L表示,可特异性结合抗原。而靠近C端(羧基端)其他部分(L链½和H链¾或⅘处)氨基酸的组成和排列顺序变化不大,称为恒定区(constant region,C区),用CH和CL表示。
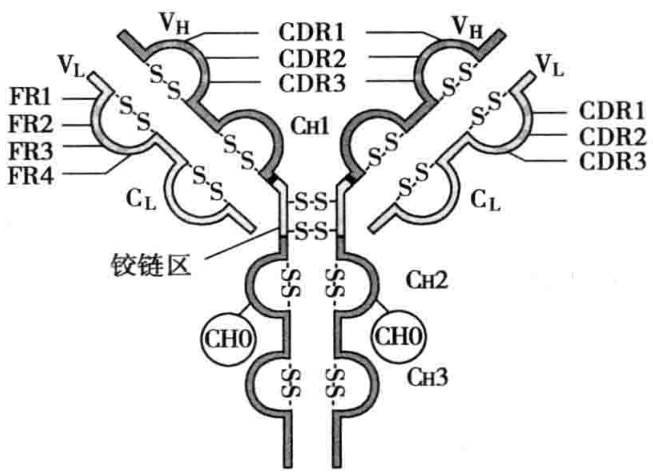
V_H和V_L各有3个区域的氨基酸组成和排列顺序高度可变,称为高变区(hypervariable region,HVR)或互补决定区(complementarity determining region,CDR),构成了抗体分子与抗原分子发生特异性结合的关键部位。在V区中,CDR之外区域的氨基酸组成和排列顺序相对较保守,称为骨架区(framework region,FR)(图3-1)。
Ig重链恒定区氨基酸的组成和排列顺序不同,故其抗原性也不同,据此可将重链分为γ、α、μ、δ及ε 5类,与之相应的Ig也分为5类或5个同种型,分别为IgG、IgA、IgM、IgD和IgE。不同类的免疫球蛋白具有不同的特征。即使同一类Ig其铰链区氨基酸组成和重链二硫键的数目、位置也不同,因此又可将同类Ig分子分为不同亚类,如人IgG可分为IgG1~4,IgA可分为IgA1~2。
Ig轻链可分为κ链和λ链,由此免疫球蛋白可分为两型,即κ型和λ型。一个天然免疫球蛋白分子上的两条轻链总是同型,而重链总是同类。人类血清中各类免疫球蛋白κ和λ型的比例约为2∶1。
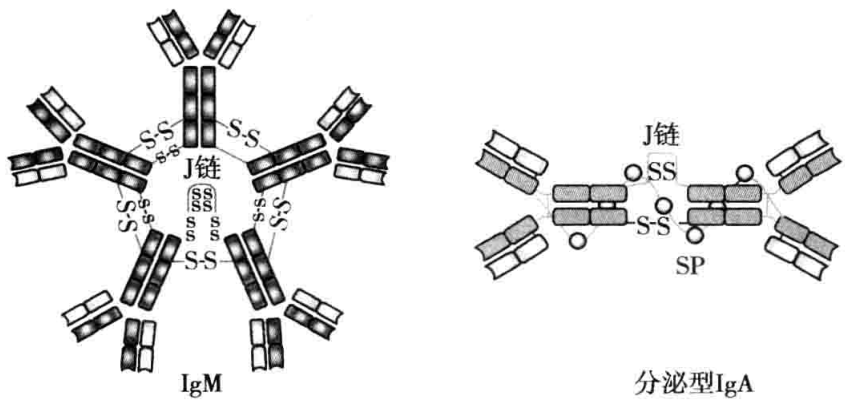
5类Ig中IgG、IgD、IgE和血清型IgA皆由1个单体组成,而分泌型IgA(sIgA)和IgM则分别由2个和5个单体通过连接链(joining chain,J链)和二硫键连接组成二聚体和五聚体(图3-2)。J链是一富含半胱氨酸的多肽链,由124个氨基酸组成,由浆细胞合成,重要功能是将单体Ig分子连接为多聚体。sIgA还含有分泌片(secretory piece,SP),为含糖肽链,以非共价形式结合于IgA二聚体上,由黏膜上皮细胞合成和分泌,并一起被分泌到黏膜表面。分泌片具有保护sIgA免受蛋白水解酶降解的作用,并介导sIgA二聚体向黏膜上皮外转运。
二、免疫球蛋白的结构域
Ig分子的多肽链可折叠成几个由二硫键连接的球形结构域,每个结构域一般具有其相应的功能。轻链有V_L和C_L两个结构域;IgG、IgA和IgD重链有VH、CH1、CH2和CH3 4个结构域;IgM、IgE比IgG多一个CH4,有5个结构域。这些结构域的功能虽不同,但其结构相似。每个结构域约由110个氨基酸组成,其氨基酸的序列具有相似性或同源性。
各结构域的功能为:
1. VL和VH是结合抗原的部位,它可与相应的抗原表位在空间结构上形成精确的互补;
2. CH1和CL具有部分同种异型的遗传标志;
3. CH2(IgG)和CH3(IgM)是结合补体部位,女性妊娠时,母体的IgG可借助CH2通过胎盘;
4. IgG的CH3可与吞噬细胞、B细胞、NK细胞表面的IgG Fc受体(FcγR)结合;IgE的C_H2和C_H3可与肥大细胞和嗜碱性粒细胞表面的IgE Fc受体(FcεRI)结合,与Ⅰ型超敏反应的发生有关。
铰链区位于CH1与CH2之间,含有丰富的脯氨酸,因此易伸展弯曲,能改变两个结合抗原的Y形臂之间的距离和位置,有利于两臂同时结合两个间距不同的抗原表位,也易使补体结合位点暴露,有利于启动补体的活化。铰链区易被木瓜蛋白酶、胃蛋白酶等水解,产生不同的水解片段(图3-3)。
三、免疫球蛋白的水解片段
用木瓜蛋白酶和胃蛋白酶水解Ig分子,是研究Ig结构与功能的重要方法之一。
木瓜蛋白酶水解Ig分子的部位是在铰链区二硫键连接的两条重链的近N端,可将Ig裂解为两个相同的抗原结合片段(fragment antigen binding,Fab)和一个可结晶片段(fragment crystallizable,Fc)(图3-4)。Fab段含有一条完整的轻链和重链N端的½部分,能与一个抗原表位特异性结合,为单价。Fc段低温下可形成结晶,含两条重链C端的½及重链间的二硫键,它不能与抗原结合,是Ig与效应分子或细胞相互作用的部位。
胃蛋白酶水解Ig分子的部位是在铰链区二硫键连接的两条重链的近C端,水解后可获得含2个Fab段的F(ab')₂片段和若干较小的pFc'片段。F(ab')₂片段能与两个抗原表位特异性结合,为双价,目前尚未发现pFc'有生物学活性。
水解后Ig的F(ab')₂片段既保留了结合相应抗原的生物学活性,又避免了Fc段免疫原性可能引起的副作用,因而作为生物制品有较大的实际应用价值。例如白喉抗毒素、破伤风抗毒素经胃蛋白酶消化后精制提纯的制品,因去掉Fc段可减缓超敏反应的发生。
分子结构示意图.png)
水解片段示意图.png)