第三节 药物代谢动力学
第三节 药物代谢动力学
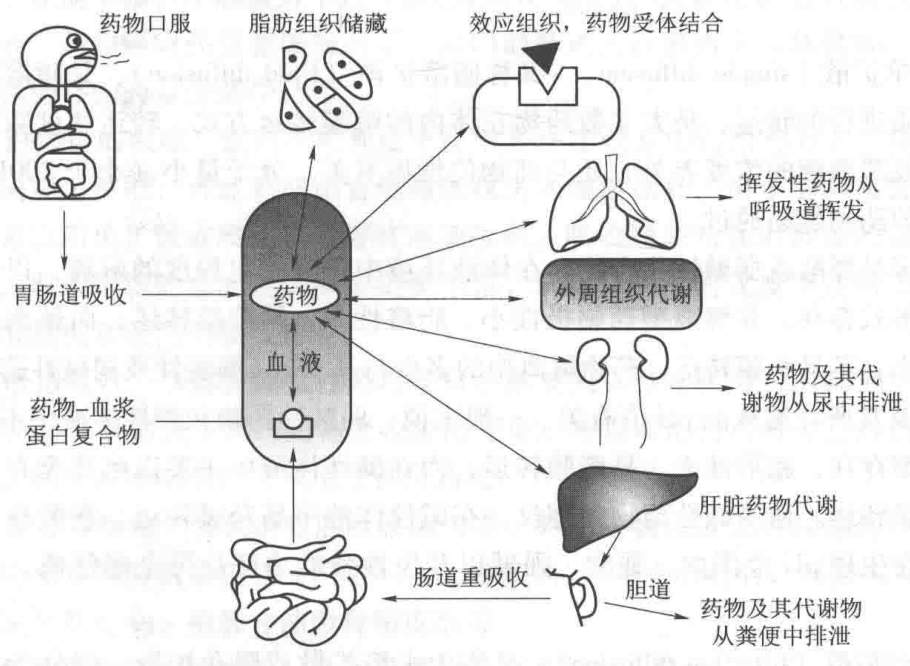
药物代谢动力学(pharmacokinetics)简称药动学,是研究药物的体内过程(包括吸收、分布、代谢和排泄),并运用数学原理和方法阐释药物在机体的动态规律。药动学是药理学的一个重要组成部分,基本过程是吸收(absorption)、分布(distribution)、代谢(metabolism)及排泄(excretion)。其中药物在体内的吸收、分布和排泄过程称为药物转运(transportation of drug),药物的代谢和排泄过程合称为药物的消除(elimination)。药物在体内的过程及动态变化规律,见图1-6所示。
图1-6 药物体内过程示意图
一、药物的体内过程
(一) 药物的跨膜转运
药物进入机体后要到达作用部位产生效应,必须通过各种生物膜,药物从生物膜的一侧转运到膜的另一侧过程,称为药物的跨膜转运。生物膜是细胞外表的质膜和细胞内的各种细胞器膜(如核膜、线粒体膜、内质网膜和溶酶体膜)的总称。生物膜由磷脂和蛋白质构成,是以液态的脂质双分子层为基架,其中镶嵌着不同生理功能的蛋白质。
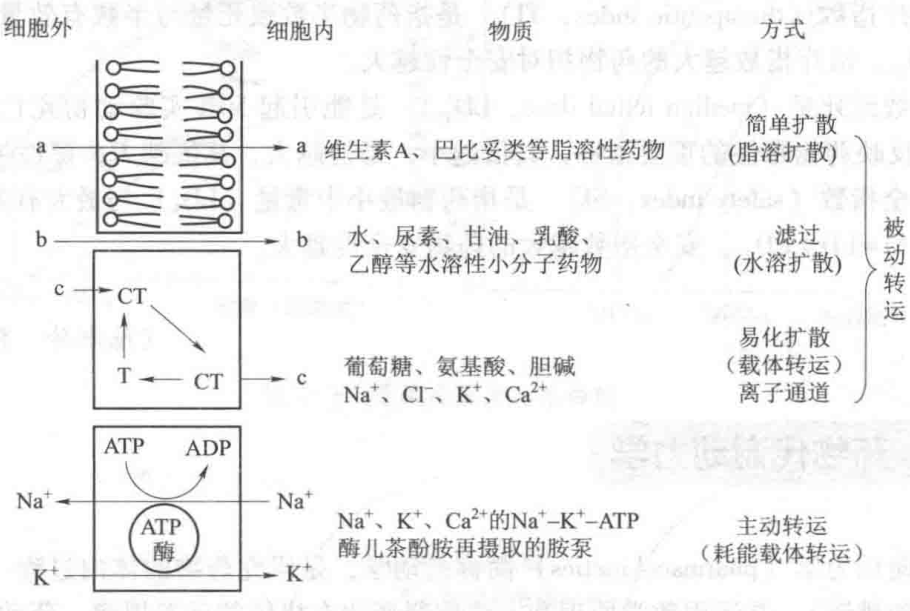
药物跨膜转运的方式主要有被动转运和主动转运两种,见图1-7。
图1-7 药物转运方式模式图
1. 被动转运 被动转运(passive transport)是指药物由高浓度侧向低浓度侧的跨膜转运,又称为顺梯度转运。此种转运不消耗能量,无饱和性,转运速度主要取决于膜两侧药物浓度差,当膜两侧药物浓度达到平衡时,转运即停止。包括简单扩散、滤过扩散和易化扩散。 (1) 简单扩散(simple diffusion) 又称脂溶扩散(lipid diffusion),是脂溶性药物通过细胞膜的脂质进行的转运,是大多数药物在体内的跨膜转运方式。转运速度除取决于膜的性质、面积及膜两侧的浓度差外,还与药物的性质有关。分子量小(小于200D)、脂溶性大、极性小的药物较易通过。
药物大多是弱酸或弱碱性化合物,在体液环境中都有一定程度的解离,以解离型和非解离型两种形式存在。非解离型药物极性小、脂溶性大,易跨膜转运;而解离型药物极性大、脂溶性小,不易跨膜转运。药物解离型的多少与其pKₐ(弱酸性或弱碱性药物解离常数的负对数)及其所在溶液的pH值有关。一般来说,弱酸性药物在酸性体液中不易解离,主要以非解离型存在,脂溶性大,易跨膜转运;而在碱性体液中主要以解离型存在,脂溶性小,不易跨膜转运。而弱碱性药物则相反,在碱性体液中易跨膜转运,在酸性体液中不易跨膜转运。在生理pH范围内,强酸、强碱以及极性强的季铵盐可全部解离,难以透过生物膜。 (2) 滤过扩散(filtration diffusion) 又称为水溶扩散或膜孔扩散,指分子直径小于膜孔的水溶性小分子药物,借助膜两侧的流体静压和渗透压差被水携带到低压侧的过程。如水、乙醇、尿素等水溶性小分子物质及O₂、CO₂等气体分子均可通过膜孔滤过扩散。细胞膜的膜孔较小,只有小分子药物可通过;毛细血管壁的膜孔较大,多数药物可通过;肾小球的膜孔更大,绝大多数药物及其代谢产物均可通过肾小球滤过而被排泄。 (3) 易化扩散(facilitated diffusion) 又称为载体转运,是指一些不溶于脂质而与机体生理代谢有关的物质如葡萄糖、氨基酸、核苷酸等借助膜上的载体,进行不耗能的顺浓度差转运。一些离子如Na⁺、K⁺、Ca²⁺等,可经细胞膜上特定的蛋白质通道由高浓度侧向低浓度侧转运,这个过程也属易化扩散。易化扩散的特点有:1. 载体具有高度特异性,每种载体只能转运特定的药物;2. 载体还具有饱和现象,当药物浓度很高时,载体被饱和,出现饱和限速现象;3. 两种由同一载体转运的药物之间存在竞争性抑制。
2. 主动转运 主动转运(active transport)是指药物依赖生物膜上的特殊载体,从低浓度侧向高浓度侧的跨膜转运,也称为逆梯度转运或“上山”转运。其特点是需要载体、消耗能量、有饱和限速性和竞争抑制现象。这种转运主要存在于神经元、肾小管和肝细胞内,而以这种方式转运的药物不多,如青霉素从肾小管分泌排泄属于此种。
(二) 药物的吸收
药物的吸收是指药物从给药部位进入血液循环的过程。除静脉(血管内)给药外,其他给药途径均存在吸收的过程。药物吸收的速度和程度直接影响药物作用的快慢和强弱。
1. 吸收途径 临床常用的血管外给药途径有消化道给药、注射给药、呼吸道给药和皮肤黏膜给药等。 (1) 消化道吸收 口服给药是临床最常用的给药方式,具有方便、安全、经济等优点。大多数药物以简单扩散的方式通过胃肠道吸收。分子量小、脂溶性大、非解离型药物较易吸收。胃液的pH为0.9~1.5,有利于弱酸性药物的吸收,但由于胃黏膜的吸收面积小,胃排空快,药物在胃内滞留时间短,所以药物实际上在胃内吸收量很少。
小肠是药物吸收的主要部位。因为小肠黏膜表面富有绒毛,绒毛上皮细胞为单细胞,吸收面积大,血流丰富,小肠液近中性(pH为4.8~8.2),大多数弱酸或弱碱性药物均易在此溶解吸收。药物经胃肠道黏膜吸收后,经门静脉进入肝脏再进入体循环。有首过消除的药物进入体循环的药量会减少。 (2) 注射部位的吸收 肌内注射和皮下注射是临床较常用的给药方式。注射后,药物沿结缔组织向周边扩散,再经毛细血管壁被吸收进入血液循环。由于毛细血管壁细胞间隙较大,药物常以简单扩散或膜孔扩散方式迅速吸收。吸收速率与注射部位的血流量及药物的剂型有关。肌肉组织的血流量比皮下组织丰富,所以肌内注射比皮下注射吸收快。水剂吸收迅速,混悬剂和油剂则吸收较慢。 (3) 呼吸道吸收 气体或挥发性药物经口、鼻吸入后经呼吸道可由肺泡吸收。肺泡表面积大(200m²),且血流丰富,药物吸收快而完全。呼吸道给药可避免首过消除,达到局部治疗目的。临床对哮喘治疗常采用此种给药法。 (4) 皮肤黏膜吸收 完整的皮肤吸收能力差,外用药物主要发挥局部作用。在药物制剂中加入透皮吸收剂后制成皮肤外用制剂(如贴皮剂),经皮给药后,可发挥局部或全身作用,如硝苯地平贴皮剂、硝酸甘油缓释贴皮剂等。
黏膜远较皮肤的吸收能力强。鼻腔黏膜的吸收面积大,且血管丰富,吸收也较迅速。有些药物还可经舌下给药或直肠给药,这两种给药途径使药物分别通过口腔黏膜和直肠黏膜吸收。舌下给药虽然吸收面积小,但血流丰富,吸收迅速,起效快,无首过消除。对于在胃肠道中不稳定或在肝中易被破坏的药物,如硝酸甘油、异丙肾上腺素等可采用此种给药途径。直肠给药,因其吸收面积很小,肠腔液体量少,pH为8.0左右,不利于多数药物溶解,吸收不如口服给药迅速和规则,但当患者处于昏迷、呕吐状态,尤其儿童不宜口服时可考虑直肠给药。
2. 影响药物吸收的因素 影响药物吸收的因素很多,除了给药途径外,主要有药物的理化性质、药物制剂、吸收环境等。 (1) 药物的理化性质 一般来说,弱酸性药物在胃中易吸收,而弱碱性药物在小肠中吸收。药物吸收程度取决于药物分子大小、离子化程度和脂溶性高低,在水和脂类中均不溶解的药物很难吸收。如硫酸钡口服时不溶解而不吸收,可用作造影剂;硫酸镁水溶液口服难吸收,常用作泻药;而水溶性钡盐口服可吸收,有剧毒。此外,药物的制剂类型也可影响吸收。一般溶液剂比片剂及胶囊剂等固体剂型吸收快。 (2) 首过消除(first pass elimination) 又称为首关效应(first pass effect),是指某些药物经口服在通过胃肠黏膜和肝脏时,部分被代谢灭活,使进入体循环的药量减少,药效降低的现象。如硝酸甘油,单次通过肝脏即有90%被灭活,故口服疗效差,需采用舌下给药、静脉滴注或经皮给药。
除硝酸甘油外,普萘洛尔、利多卡因、丙米嗪、吗啡、维拉帕米及氯丙嗪等也均具有明显的首关效应,使用时应注意。 (3) 吸收环境 胃排空速度、肠蠕动快慢、胃内容物的多少和性质均可影响药物吸收。胃肠蠕动增加、排空快或肠内容物多,可阻碍药物与吸收部位的充分接触,使吸收的速度和程度均减少。油和脂肪等食物,可促进脂溶性药物的吸收。
(三) 药物的分布
药物的分布是指吸收后的药物随着血液循环到达各组织器官的过程。大多数药物在体内的分布是不均匀的,存在明显的选择性。影响药物分布的因素主要有以下几个方面。
1. 药物与血浆蛋白结合 吸收进入血液循环的药物可与血浆蛋白(主要是白蛋白)进行可逆性结合。与血浆蛋白结合的药物称为结合型药物,未与血浆蛋白结合的药物称为游离型药物。结合型药物分子量大,不能通过生物膜进行跨膜转运,暂时失去药理活性,不被代谢和排泄,成为药物在血液中一种暂时的储存形式,当血浆中游离型药物的浓度随着其分布和消除降低时,结合型药物可释放出游离型药物,结合与游离两个过程保持着动态平衡。与血浆蛋白结合率高的药物,不易分布,起效慢,但在体内消除也慢,作用维持时间较长。
药物与血浆蛋白的结合具有饱和性,当药物浓度过高时,与血浆蛋白的结合达到饱和,会使游离型药物浓度增高,导致药效增强,甚至出现毒性反应。药物与血浆蛋白的结合是非特异性的,两种或两种以上的药物可竞争性地与同一蛋白结合而发生置换现象,被置换出来的游离型药物浓度增高,药效或毒性随之增强。如口服抗凝血药华法林后再服用解热镇痛药保泰松,可使血中华法林游离浓度成倍增加(前者血浆蛋白结合率为99%,后者为98%),导致抗凝作用增强,引起出血反应。在联合用药时,应注意避免由此造成的毒性反应。
在某些病理情况下,血浆蛋白减少,如肝硬化、慢性肾炎、尿毒症、极度营养不良等,药物与血浆蛋白结合减少,游离型药物增多,也易引起毒性反应。
2. 药物的理化性质和体液的pH 脂溶性药物和水溶性小分子药物易通过生物膜而分布,水溶性大分子药物则难通过生物膜分布。生理情况下,细胞外液pH为7.4,细胞内液pH为7.0,由于pH的差异导致药物解离度的不同,故弱酸性药物在细胞外液浓度较高,弱碱性药物则相反,在细胞内浓度较高。通过改变血液pH,可改变药物的分布方向。如在抢救巴比妥类(弱酸性)药物中毒时,可用碳酸氢钠碱化血液和尿液,不仅可促进药物由脑细胞向血液转运,又可减少药物在肾小管的重吸收,加速药物从尿液排出,使病人迅速脱离危险。
3. 局部器官血流量 吸收的药物通过血液循环迅速向全身组织器官转运,药物首先分布于肝、肾、脑、心等血流量相对较大的器官组织,然后再分布到肌肉、皮肤或脂肪等血液灌注量相对较小的组织,这种现象称为药物的再分布。脂肪组织的血流量虽较少,但其面积大,是脂溶性药物的巨大储库。如静脉注射硫喷妥钠后,因其脂溶性高,首先分布到富含类脂质的脑组织,迅速产生麻醉作用,随后药物迅即从脑向脂肪组织转移,作用很快消失。
4. 药物与组织的亲和力 药物对某些组织的亲和力,使药物在该组织中的分布浓度明显高于其他组织。如碘主要集中在甲状腺;钙沉积于骨骼中;汞、砷、锑等重金属和类金属在肝、肾中分布较多,中毒时可损害这些器官。有时药物分布多的一些组织,并非药物的作用部位,而与药物的毒性有关。如四环素与钙络合沉积于骨骼与牙齿中,可使儿童骨骼和牙齿的正常生长发育受到抑制。
5. 特殊屏障 药物在血液与器官组织之间转运时所受到的阻碍称为屏障。体内影响药物分布的屏障主要有血-脑屏障和胎盘屏障。 (1) 血-脑屏障(blood-brain barrier, BBB) 主要是指血液与脑组织、血液与脑脊液间的屏障,其能阻碍药物进入脑中,有利于维持中枢神经系统内环境的相对稳定。这主要是由于脑毛细血管内皮细胞间连接紧密,间隙较小,基膜外还有一层星状胶质细胞包绕,只有分子量小、脂溶性高的药物可以通过被动转运,进入脑组织。新生儿血-脑屏障尚未发育完全,其中枢神经易受药物的影响。当脑膜炎症时,血-脑屏障通透性增加,此时应用大剂量磺胺嘧啶、青霉素等,可在脑脊液中达到有效治疗浓度而发挥作用。 (2) 胎盘屏障(placental barrier) 是指胎盘绒毛与子宫血窦间的屏障,它能将母体与胎儿血液隔开。胎盘屏障的通透性与一般生物膜无明显差异,几乎所有药物都能通过胎盘屏障进入胎儿体内,只是程度和快慢不同而已。因此孕妇用药应谨慎,以防胎儿中毒或致畸。
(四) 药物的代谢
药物的代谢是指药物在体内发生化学结构的变化,也称为药物的生物转化或转化(biotransformation)。药物的代谢主要在肝脏进行,少数药物也可在肠、肾、血浆等部位进行。
1. 药物代谢的意义 药物代谢的意义主要使药物活性改变。大多数药物经代谢后由活性药物转化为无活性代谢物,称为“灭活”(inactivation);少数药物可由无活性或活性较低的药物变成有活性或活性强的药物,称为“活化”(activation),如抗癌药环磷酰胺,进入体内转化为磷酰胺氮芥后呈现抗癌作用。这种经代谢后才能产生药理效应的药物称为前药(prodrug);还有少数药物由无毒或毒性小的药物变成毒性代谢物,如异烟肼经肝脏代谢后生成的乙酰异烟肼对肝脏有较强的毒性。多数脂溶性药物,经代谢后转化为水溶性高的代谢物,不易被肾小管重吸收,以利于从肾脏排出。某些水溶性高的药物,在体内也可不转化,以原形从肾脏排泄。药物代谢的最终目的是促使药物排出体外。
2. 药物代谢的方式 药物在体内代谢的方式有氧化、还原、水解和结合。其中氧化、还原和水解反应为第Ⅰ相反应,结合反应为第Ⅱ相反应。药物经过第Ⅰ相反应,多数被灭活,但也有少数被活化,故药物的代谢不能简单地称为解毒过程。第Ⅱ相反应,是经Ⅰ相反应生成的代谢物或某些原形药物,可与体内的葡萄糖醛酸、硫酸、乙酰基、甲基、甘氨酸等结合,结合后的代谢物药理活性降低或消失,水溶性增大,易于经肾脏排出。各种药物体内代谢的途径和方式也各不相同。
3. 药物代谢的酶 药物代谢需要酶的参与,根据存在部位将其分为微粒体酶和非微粒体酶两类。 (1) 微粒体酶 存在于肝细胞内质网中,是促进药物代谢的主要酶系统,又称为肝药酶,如细胞色素P450(由于其与一氧化碳结合后的吸收主峰在450nm处而得名,简称CYP)。细胞色素P450是一个庞大的多功能酶系,由多种酶组成,在内源物和外源物的代谢过程中起重要作用。其主要特点是:1. 选择性低,能催化多种药物代谢;2. 个体差异大,存在明显的种族、性别、年龄等的差异;3. 活性和数量有限,在同时被转化的药物间容易发生竞争性抑制;4. 酶活性易受药物的影响而表现出增强或减弱。 (2) 非微粒体酶 存在于血浆、细胞质和线粒体中的多种酶,主要促进水溶性较大、脂溶性较小的药物以及结构与体内正常代谢物类似的物质的代谢,如单胺氧化酶、胆碱酯酶等。
4. 肝药酶的诱导与抑制 肝药酶的活性和数量是不稳定的,易受某些药物的影响。 (1) 药酶诱导剂 是指能使肝药酶活性增强或合成加速的药物,如苯巴比妥、苯妥英钠、利福平、地塞米松等。可加速药物自身和其他药物的代谢,使药效降低。药酶诱导作用可解释某些药物连续应用产生的耐受性、交叉耐受性、药物相互作用等现象。如苯巴比妥的药酶诱导作用很强,连续应用可加速自身代谢,易产生耐受性;将苯巴比妥与口服抗凝药华法林合用时,可加速华法林代谢,使其作用减弱。 (2) 药酶抑制剂 是指能使肝药酶活性降低或合成减少的药物,如氯霉素、异烟肼、西咪替丁等。药酶抑制剂能减慢其他药物的代谢,使药效增强,如氯霉素与苯妥英钠合用,可使苯妥英钠的代谢减慢而作用增强,甚至出现毒性反应。
(五) 药物的排泄
药物的排泄是指药物及其代谢产物通过排泄器官排出体外的过程。药物排泄速度的快慢可直接影响药物的作用强度和持续时间。药物排泄的主要器官是肾脏,其次是胆道、呼吸道、乳腺、汗腺、唾液腺等。
1. 肾脏排泄 药物经肾脏排泄的方式有肾小球滤过、肾小管分泌及肾小管重吸收三种方式。肾小球毛细血管的膜孔较大,血流丰富,滤过压高,故通透性大。除了与血浆蛋白结合的药物外,游离型药物及其代谢产物均可经过肾小球滤过进入肾小管腔内。脂溶性大、极性小、非解离型药物和代谢产物经肾小管上皮细胞可以重吸收入血。改变尿液的pH,可以改变弱酸性或弱碱性药物的解离度,从而改变药物的重吸收程度。当尿液呈酸性时,弱酸性药物主要以非解离型存在,脂溶性高,重吸收多,排泄慢,而弱碱性药物在酸性尿中则排泄快;反之,当尿液呈碱性时,弱酸性药物排泄快,而弱碱性药物排泄慢。临床上可利用改变尿液pH的方法加速药物的排泄以治疗药物中毒。如水杨酸类药物过量中毒时,可应用碳酸氢钠碱化尿液以促进药物排泄。另外,增加尿量可降低尿液中药物的浓度,减少药物的重吸收,加速排泄。
有少数药物可通过肾小管分泌排泄,这是一个主动转运过程,需非特异性载体转运系统完成。肾小管上皮细胞存在有机酸和有机碱两类转运系统,前者转运弱酸性药物,后者转运弱碱类药物。载体选择性低,若两种药物通过同一载体转运时,彼此间可发生竞争性抑制。如丙磺舒可抑制青霉素、吲哚美辛等的主动分泌,使被抑制药排泄减少,作用增强,持续时间延长。
当肾功能不全时,主要经肾脏排泄的药物排泄减慢,血药浓度升高,作用增强,且可能引起蓄积中毒,应适当减少剂量或延长给药间隔时间。
2. 胆汁排泄 有些药物及其代谢产物可经肝脏通过胆汁排泄进入十二指肠,再经粪便排出体外。有些药物随胆汁到达小肠后可在肠道内被重吸收,这一现象称为肝肠循环(hepato-enteral circulation)。肝肠循环可使血药浓度下降减慢,药物作用时间延长。如洋地黄、地西泮等药物肝肠循环现象明显。有些抗生素如红霉素、利福平等经胆汁排泄,在胆道内浓度高,可作为胆道感染的治疗药物。
3. 其他途径排泄 (1) 肺排泄 肺脏是某些挥发性药物的主要排泄途径,如吸入麻醉药恩氟烷、异氟烷、氧化亚氮等主要经肺排出;饮酒后可从呼出的气体中检出乙醇含量。 (2) 经乳汁排泄 人乳汁较血液偏酸性(pH为6.8~7.3)且富含脂质。有些脂溶性高及弱碱性药物如吗啡、阿托品等可经乳汁排泄,乳汁中药物浓度高,直接影响乳婴。故哺乳期妇女用药应慎重。
有些药物还可以通过唾液、汗液、泪液等排泄。药物在唾液中的浓度与血药浓度有一定相关性,故临床偶有以唾液代替血液样本,进行血药浓度监测。
二、药物代谢动力学基本概念
(一) 血药浓度-时间曲线
药物在体内的吸收、分布、代谢和排泄是一个连续变化的动态过程,可用体内药量或血药浓度随时间变化来表示这一动态过程。在给药后不同时间采血,测定血药浓度,以血药浓度为纵坐标,时间为横坐标,可绘出血药浓度-时间曲线(drug concentration-time curve),简称药-时曲线,也称为时-量曲线。
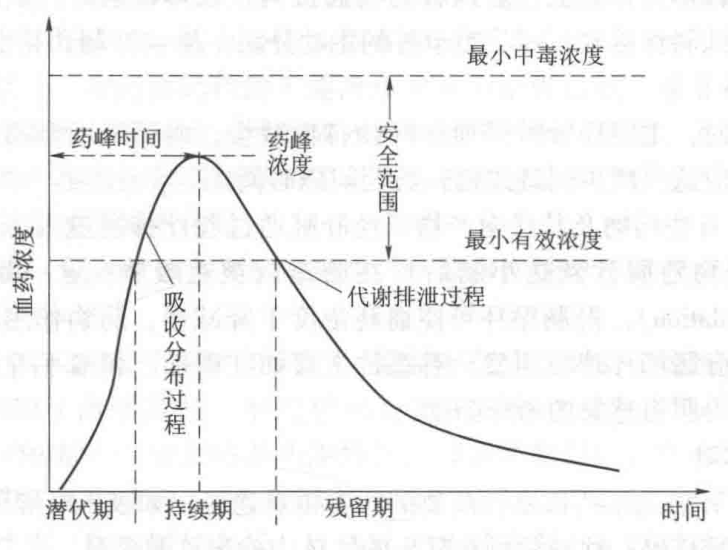
非静脉途径给药的药-时曲线,如图1-8所示。一般可分为三期:潜伏期、持续期和残留期。
图1-8 单次肌内注射给药的药-时曲线
潜伏期(latent period) 指用药后到开始出现作用的一段时间,主要反映药物的吸收和分布过程。静脉注射给药一般无潜伏期。持续期(persistent period) 是指药物维持有效浓度的时间,其长短取决于药物的吸收和消除速度。药峰浓度(Cₘₐₓ) 是指用药后所能达到的最高浓度,通常与给药剂量成正比。药峰时间(Tₘₐₓ) 是指用药后达到药峰浓度的时间。残留期(residual period) 是指体内药物浓度已降至最小有效浓度以下,但又未从体内完全消除。残留期的长短与消除速度有关,残留期长,反映药物消除慢,反复应用易引起蓄积中毒。从图中还可测出药物的最小有效浓度和最小中毒浓度,以此确定安全范围。
药-时曲线的形态可反映药物吸收与消除的情况。曲线上升段斜率大,则吸收快,斜率小,吸收慢;曲线下降段坡度陡峭则消除快,坡度平缓则消除慢。药峰浓度与药峰时间,可分别反映药物吸收的程度与速度。
药-时曲线下面积(area under concentration-time curve, AUC) 是坐标横轴与药-时曲线围成的面积。它表示一次服药后某段时间内的药物吸收总量,是评价药物吸收程度的一个重要参数,常被用于计算药物制剂的生物利用度。
时-效曲线(time-effect curve) 是以药物效应为纵坐标,时间为横坐标绘制的曲线。该曲线的形态与分期与药-时曲线基本相似。
(二) 生物利用度
生物利用度(bioavailability, F) 是指药物被吸收进入血液循环的速度和程度的一种量度。它是评价药物制剂质量的重要参数,与药物起效快慢和作用强弱密切相关。药物制剂因素如药物颗粒的大小、晶型、赋形剂、生产工艺等的不同以及给药途径均可影响生物利用度,从而影响药物疗效。
生物利用度可用给予一定剂量的药物后,药物被机体吸收的百分率来表示。 F = A / D × 100% A为进入体循环的药物总量,实际工作中通常用给药后药-时曲线下面积AUC表示;D为用药剂量,通常用血管内给相同剂量药物所得的AUC表示。静脉注射后药物全部进入血循环,F = 100%;其他各种给药途径,存在吸收过程,因各因素影响,F < 100%。根据比较标准的不同,生物利用度可分为绝对生物利用度和相对生物利用度,其计算方式为:
绝对生物利用度 F(%) = 口服制剂AUC / 静注制剂AUC × 100% 相对生物利用度 F(%) = 被试制剂AUC / 参比制剂AUC × 100%
绝对生物利用度可用于评价同一药物不同给药途径的吸收率大小;相对生物利用度则可用于评价不同生产厂家同一制剂的吸收率差异或同一厂家的不同批号药品间的吸收率差异。
(三) 表观分布容积
表观分布容积(apparent volume of distribution, Vd) 是指药物在体内分布达到动态平衡时,体内药量与血药浓度的比值。计算公式为: Vd (L) = 体内总药量 (A) (mg) / 血药浓度 (C) (mg/L)
表观分布容积并不代表真正的生理体积,只是一个理论容积,是便于进行体内药量与血药浓度互换运算的一个比值。但其可反映药物在体内分布的广泛程度以及组织结合程度。Vd值小,可推测药物大部分分布于血浆中,组织内药量少;Vd值大,表明血药浓度低,药物分布广泛或组织摄取多。此外,利用Vd,可推算体内的药物总量或求算达到某一有效血药浓度时的药物剂量。
(四) 清除率
清除率(clearance, Cl) 是指单位时间内,多少体积血浆中药物从体内被清除,其单位为ml·min⁻¹或L·h⁻¹。Cl是反映药物自体内消除的一个重要指标,其与消除速率常数及分布容积的关系可用下式表示: Cl = K · Vd Cl是肝、肾等消除药物的总和,它可反映肝、肾功能,当功能不良时,Cl值会下降。临床上根据已知药物的有效浓度,利用Cl值,可确定给药剂量。
(五) 药物的消除动力学类型
药物消除动力学过程是指药物在体内经代谢和排泄,使血药浓度不断降低的动态变化过程,其规律可用消除速率与血药浓度关系的数学方程式表达即:dC/dt = -kCⁿ。
式中C表示血药浓度,t为时间,dC/dt为消除速率,k是消除速率常数,负号表示血药浓度随时间变化而降低,当n=1时即为一级动力学过程,n=0时为零级动力学过程。
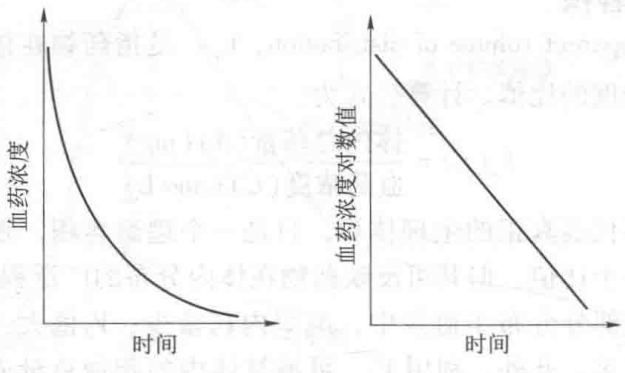
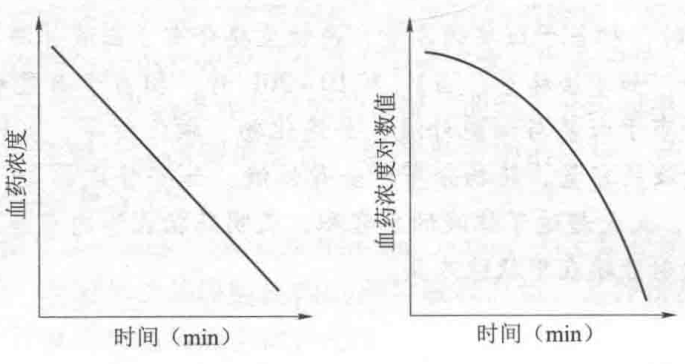
1. 一级动力学消除 当n=1时,dC/dt = -kCⁿ = -kC。 式中k为一级动力学消除速率常数,单位是h⁻¹;它不表示单位时间内消除的实际药量,而是体内药物瞬时消除的百分率。一级动力学消除的特点是药物消除速率与血药浓度成正比,血药浓度高,单位时间内消除的药量多,当血药浓度降低后,药物消除速率也按比例下降,即单位时间内消除恒定比例的药物,故又称恒比消除。绝大多数药物在体内按此方式消除。其药时曲线的下降部分在半对数坐标上呈直线,见图1-9,故又称线性动力学。
图1-9 一级动力学在普通坐标系和对数坐标系上的药-时曲线
2. 零级动力学消除 n=0时,dC/dt = -kC⁰ = -k。表明药物的消除速率与血药浓度无关,单位时间内消除恒定数量的药物,故又称恒量消除。由于其药-时曲线下降部分在半对数坐标上呈曲线,见图1-10,故又称非线性消除。当用药量超过机体最大消除能力时或机体消除能力低下时,药物按零级动力学消除。
图1-10 零级动力学在普通坐标系和对数坐标系上的药-时曲线
(六) 半衰期
1. 半衰期的概念 半衰期(half life time, t₁/₂) 通常指血浆半衰期,即血浆药物浓度下降一半所需的时间。半衰期可反映药物在体内的消除速度,消除快的药物,其半衰期短,消除慢的药物,半衰期长。由于大多数药物在体内是按一级动力学方式消除,其半衰期是一个常数,见表1-1。计算公式为:t₁/₂ = 0.693 / k,式中k为消除速率常数。
| 半衰期数 | 体存药量(%)(一次给药) | 消除药量(%)(一次给药) | 消除药量(%)(连续恒速、恒量给药) | 累积药量(%)(连续恒速、恒量给药) |
|---|---|---|---|---|
| 1 | 50.00 | 50.00 | 50.00 | 50.00 |
| 2 | 25.00 | 75.00 | 75.00 | 75.00 |
| 3 | 12.50 | 87.50 | 87.50 | 87.50 |
| 4 | 6.25 | 93.75 | 93.75 | 93.75 |
| 5 | 3.13 | 96.87 | 96.87 | 96.87 |
| 6 | 1.56 | 98.44 | 98.44 | 98.44 |
表1-1 恒比消除药物的消除与积累
2. 半衰期的临床意义 (1) 是确定临床给药间隔的重要依据。t₁/₂长的药物,给药间隔时间长;t₁/₂短则给药间隔时间短。通常给药间隔时间约为一个半衰期。 (2) 作为药物分类的依据。根据半衰期的长短,可将药物分为长、中、短效等类药。 (3) 预测药物达到稳态血药浓度的时间。连续恒速给药时,约经过4~5个t₁/₂,可达到稳态血药浓度。 (4) 预测药物从体内基本消除的时间。一次给药后,经过5个t₁/₂,体存药量在5%以下,可认为药物已基本消除。
t₁/₂常受到机体肝肾功能状态的影响,肝肾功能不良者,绝大多数药物t₁/₂延长,用药时应予注意。
(七) 多次用药的药-时曲线与稳态血药浓度
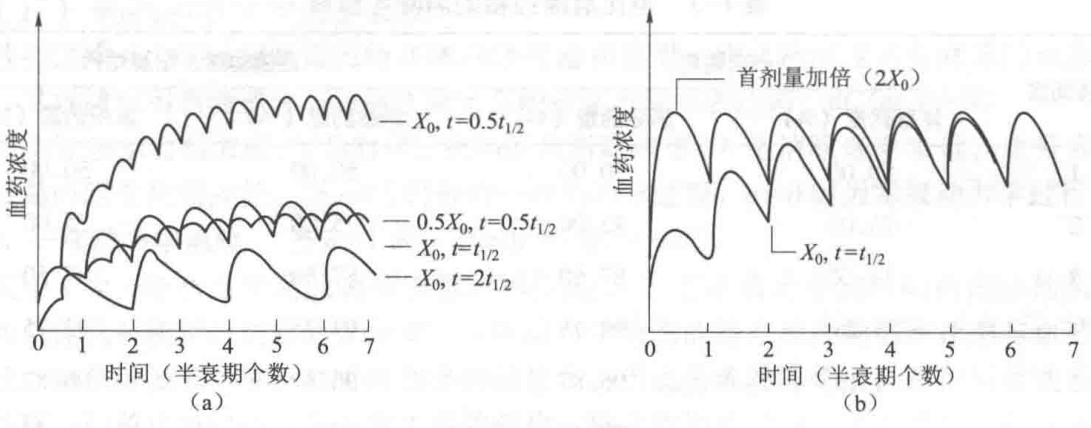
临床治疗中多数药物常需连续多次给药,方能维持有效血药浓度,以达预期疗效。当每次用药剂量(X₀)和给药间隔时间(T)均相同时,给药过程中血药浓度可依次递增,药-时曲线呈锯齿形上升,约经过5个半衰期,当给药速度与消除速度达到平衡时,血药浓度将在一个相对稳定水平范围内波动,此血药浓度称为**稳态血药浓度(steady state concentration, Cₛₛ)**,又称坪浓度(plateau concentration)或坪值(plateau)。其药-时曲线,见图1-11。
坪浓度是多次用药的常用指标之一,对于指导临床用药有实际意义。 (1) 坪浓度的高低与一日的给药总量成正比。一日给药剂量越大,坪浓度越高,剂量加倍,坪浓度也提高1倍。因此调整一日用药总量,可改变坪浓度的高低。若一日总量不变,而增加或减少给药次数则坪浓度不变,见图1-11(a)。因此,临床上小儿用药常规定1日总量,分几次给药可酌情而定。 (2) 坪浓度峰谷的波动范围与每次用药量及用药间隔成正比。一日给药总量不变,服药次数越多,每次用药量越小,血药浓度的波动也越小。对于安全范围较小的药物,宜采用少量多次分服的给药方案。 (3) 可预测药物达坪时间和基本消除时间。达坪时间约为45个t₁/₂;单次给药或停药45个t₁/₂,体内药物可基本消除。 (4) 采取首剂加倍(负荷剂量)的给药方法可迅速达到坪浓度。即首次剂量给予负荷剂量(2X₀),然后再给予维持剂量(X₀),按t₁/₂给药,经给药1次即可达坪浓度,见图1-11(b)。临床上对于危重患者可采取此种给药方式。
图1-11 多种方法给药(a)和首剂加倍给药(b)对稳态血药浓度的影响