第二节 药物效应动力学
第二节 药物效应动力学
药物效应动力学简称药效学,是研究药物对机体的作用、作用机制以及药物剂量与效应之间关系的规律。药效学既是药物作用的理论基础,也是临床合理用药的依据。
一、药物的基本作用
(一) 药物作用的性质和方式
1. 药物作用与药理效应 药物作用(drug action)是指药物与机体生物大分子(酶受体、离子通道等)间的初始作用,例如肾上腺素与心肌细胞的β受体结合并使之兴奋;药理效应(drug effect)是药物作用所引起的机体功能的继发性变化,例如肾上腺素引起的心肌收缩力增强。药物作用是动因,药理效应是结果。由于两者意义相近,所以常相互通用。
2. 药物作用的性质 药物对机体的作用,主要是调节机体组织器官原有的功能,包括兴奋和抑制两种基本作用。凡能使机体组织器官功能增强的作用称为兴奋(excitation),能产生兴奋作用的药物称为兴奋药,如咖啡因能提高中枢神经系统的功能活动,使人精神振奋,思维活跃。能使机体组织器官功能减弱的作用称为抑制(inhibition),具有抑制作用的药物称为抑制药,如地西泮能降低中枢神经系统的功能活动,引起镇静催眠。同一种药物对不同的组织器官可产生不同的作用。例如阿托品对内脏平滑肌是抑制作用,使其松弛;但对心脏却是兴奋作用,可使心率加快。兴奋作用和抑制作用在一定条件下可相互转化,例如中枢神经系统过度兴奋可导致惊厥,持续惊厥可导致衰竭性抑制,甚至死亡。
3. 药物作用的方式 药物作用的方式一般分为局部作用和吸收作用。药物无需吸收而在用药部位所呈现的作用,称为局部作用(local action),如口服氢氧化铝在胃内产生的中和胃酸作用。吸收作用(absorptive action)又称为全身作用(general action),是指药物吸收进入血液循环,而后分布到机体有关部位所呈现的作用,如口服阿司匹林产生的解热镇痛作用;舌下含服硝酸甘油出现的抗心绞痛作用等。吸收作用是绝大多数药物在体内的作用方式。
(二) 药物作用的选择性和双重性
1. 药物作用的选择性 药物进入机体后,对某些组织器官产生明显作用,而对另一些组织器官的作用很弱甚至无作用,称为药物作用的选择性(selectivity)。如强心苷类药物对心肌具有明显的兴奋作用,而对骨骼肌和平滑肌则无作用。选择性高的药物大多药理活性较高,作用范围窄,应用时针对性强,不良反应较少;选择性低的药物,作用范围广,应用时针对性不强,不良反应常较多。
药物作用的选择性是相对的,常与剂量相关。如治疗量的强心苷选择性作用于心脏,随着剂量增加也可作用于神经系统,引起头痛、失眠、视觉障碍等不良反应;又如小剂量阿司匹林有抗血小板聚集的作用,剂量加大则产生解热镇痛、抗炎抗风湿作用。一般临床应用的所有药物中,几乎没有单一作用的药物。药物作用的选择性是药物分类的基础,也是临床选择用药的依据。
2. 药物作用的双重性 药物进入机体后,既可产生对机体有利的防治作用(preventiveand therapeutic effect),又可生对机体不利的不良反应(adverse drug reaction, ADR),这就是药物作用的双重性。在临床用药时,应充分发挥药物的防治作用,尽量减少药物不良反应的发生。
(1) 防治作用 防治作用包括预防作用和治疗作用。预防作用是指提前用药以防止疾病或症状发生的作用。例如服用维生素D预防佝偻病。治疗作用是指符合用药目的或能达到治疗效果的作用。根据治疗目的不同,可分为对因治疗(etiological treatment) 和对症治疗(symptomatic treatment)。 凡能消除致病原因的治疗称为对因治疗或称为治本。例如发生感染性疾病时,使用抗生素杀灭病原微生物,属于对因治疗;凡能改善疾病症状的治疗称为对症治疗或称为治标。例如发生高热时,使用解热镇痛药使体温恢复正常,属于对症治疗。应辨证地看待对因治疗和对症治疗,通常情况下,对因治疗比对症治疗重要,但在哮喘、惊厥、休克等严重急症情况下,对症治疗比对因治疗更为迫切和重要。
(2) 不良反应 不良反应是指不符合用药目的并给患者带来不适或痛苦的反应。可分为以下几类。
副作用(side reaction) 是指药物在治疗剂量下出现的与用药目的无关的作用。其产生原因是药物的选择性低、作用广泛,当其中一种作用作为治疗作用时,其他无关作用则为副作用。副作用是药物固有的药理作用,一般比较轻微,对机体的危害不大。副作用通常可预知,但较难避免,可设法纠正,例如用麻黄碱治疗支气管哮喘时会引起中枢兴奋而失眠,同时服用催眠药可纠正。副作用和治疗作用可随着治疗目的不同而相互转化,例如阿托品具有松弛内脏平滑肌和抑制腺体分泌的作用,当用于治疗内脏绞痛时,其松弛内脏平滑肌为治疗作用,而抑制腺体分泌引起的口干为副作用;当用于麻醉前给药时,其抑制腺体分泌作用为防治作用,而松弛内脏平滑肌引起的腹胀和尿潴留则成了副作用。
毒性反应(toxic reaction) 是指用药剂量过大或用药时间过长,药物在体内蓄积过多时发生的危害机体的反应。毒性反应可因剂量过大立即发生,称为急性毒性(acute toxicity),多损害呼吸、循环及神经等系统功能;也可因长期用药,药物在体内蓄积后逐渐产生,称为慢性毒性(chronic toxicity),常损害肝、肾、骨髓、内分泌等功能。毒性反应是药物药理作用的延伸,通常也可预知。
变态反应(allergic reaction) 又称为过敏反应,是指机体受药物刺激所产生的异常免疫反应,可引起机体生理功能障碍或组织损伤。如药物热、皮疹、接触性皮炎、溶血性贫血、过敏性休克等。变态反应与药物剂量无关,在治疗量或极少量时即可发生,如微量的青霉素可引起过敏性休克。变态反应见于少数过敏体质的病人,致敏物质可能是药物本身,或是药物在体内的代谢物,甚至是药物制剂中的杂质。由于变态反应大多不易预知,因此对于易致变态反应的药物或过敏体质的病人,用药前应详细询问病人的过敏史,并做皮肤过敏试验,凡有过敏史或过敏试验阳性者,禁用有关药物。
继发反应(secondary reaction) 是由于药物治疗作用引起的不良后果,又称治疗矛盾。如长期应用广谱抗生素,由于敏感菌被抑制,一些不敏感的细菌大量繁殖而引起继发性感染,称二重感染。
后遗效应(residual effect) 是指停药后血浆药物浓度已降至最低有效浓度以下时仍残存的药理效应。如应用长效巴比妥类催眠药后,次晨仍有困倦、头昏、乏力等“宿醉”现象。
停药反应(withdrawal reaction) 是指长期服用某种药物,突然停药后原有疾病复发或加重的反应,又称为反跳反应(rebound reaction)。如长期服用普萘洛尔治疗高血压,若突然停药会导致血压急剧回升。临床对这类药物,如需停药,应逐步减量,以免发生危险。
特异质反应(idiosyncratic reaction) 是指某些药物可使少数患者出现与常人不同的特异性不良反应。如少数葡萄糖-6-磷酸脱氢酶缺乏的病人,在应用有氧化作用的伯氨喹、磺胺等药物时,可能引起溶血。特异质反应大多是由于机体生化机制异常所致,与遗传有关,属于遗传性生化缺陷。
“三致反应” 是指致畸(teratogenesis)、致癌(carcinogenesis)、致变(mutagenesis),是药物引起的特殊毒性反应,属于慢性毒性范畴,常用于评价药物的安全性。药物造成细胞DNA分子中碱基对发生改变,引起基因变异,称为致突变;突变发生在体细胞,导致恶性肿瘤的形成,称为致癌;突变发生在胚胎细胞,影响胚胎的正常发育,引起畸变,称为致畸。
二、药物作用机制
药物的作用机制(mechanism of drug action)是说明药物为什么能起作用以及如何产生作用,是药效学研究的重要内容。明确药物的作用机制,有助于理解药物的治疗作用和不良反应的本质,为临床合理用药提供理论基础。
(一) 非特异性药物作用机制
非特异性药物作用机制主要与药物的理化性质如溶解度、解离度、渗透压、表面张力等有关,是通过化学反应或物理作用改变细胞周围的理化条件而产生药理效应。如口服氢氧化铝等抗酸药(弱碱性化合物)可中和胃酸,治疗消化性溃疡;静脉注射甘露醇可提高血浆渗透压引起组织脱水而消除脑水肿;使用二巯基丙醇等络合剂与砷、汞等发生络合反应,解救其中毒等。
(二) 特异性药物作用机制
特异性药物作用机制与药物的化学结构密切相关,大多数药物属于此类。通过自身结构的特异性,影响酶、受体、离子通道、载体分子等靶点而产生一系列生理、生化反应。
1. 影响酶的活性 酶是细胞生命活动的重要物质,许多药物通过影响酶的活性而呈现作用。如新斯的明通过抑制胆碱酯酶的活性而产生拟胆碱作用;卡托普利通过抑制血管紧张素转换酶,产生抗高血压作用;尿激酶可激活血浆纤溶酶原而溶解血栓。
2. 参与或干扰细胞代谢过程 有些药物通过补充生命代谢物质的不足,治疗相应缺乏症。如维生素C治疗坏血病、铁剂治疗贫血等。另有一些药物化学结构与正常代谢物非常相似,可进入代谢过程而呈现抗代谢效应。如甲氨蝶呤的化学结构与叶酸相似,通过干扰核酸和蛋白质的合成而产生抗癌作用。
3. 影响细胞膜离子通道 细胞膜上有许多离子通道,如无机离子Na⁺、K⁺、Ca²⁺、Cl⁻等。有些药物可直接作用于这些通道,而影响离子进行跨膜转运,产生药理作用。如硝苯地平通过阻滞钙通道,抑制Ca²⁺内流,降低细胞内Ca²⁺浓度而使血管扩张,血压下降;局部麻醉药抑制Na⁺通道,阻断神经传导,产生局部麻醉作用。
4. 影响生理物质 生理物质包括自体活性物质、神经递质和激素等。有些药物通过影响生理物质的合成、贮存、释放、灭活等过程而发挥作用。如解热镇痛药可抑制体内前列腺素的生物合成而产生解热镇痛抗炎作用;磺酰脲类通过促进胰岛素的释放产生降血糖作用。
5. 影响核酸代谢 如磺胺类药物通过抑制细菌核酸的合成,而抑制细菌的生长繁殖。
6. 影响免疫功能 许多疾病涉及免疫功能。免疫抑制药(环孢素)及免疫增强药(左旋咪唑)通过影响免疫功能产生药理效应,前者用于器官移植的排斥反应,后者用于免疫缺陷性疾病的治疗。
7. 作用于受体 随着分子药理学的发展,对受体认识的不断深入,现已证实许多药物是通过激动或拮抗相应的受体而发挥作用的。
三、药物与受体
受体(receptor)理论是药效学的基本理论之一,它从分子水平阐明生命现象的生理和病理过程,是解释药物的作用、作用机制、构效关系的一种基本理论。
(一) 受体的概念和特性
1. 受体的概念 受体是存在于细胞膜、细胞质或细胞核上的大分子蛋白质,能识别、结合特异性配体并引起特定的生理效应。配体(ligand)是指能与受体特异性结合的物质,有内源性配体(包括神经递质、激素、自体活性物质等)和外源性配体(主要是药物)。配体仅与受体大分子中的一部分结合,该结合部位称为受点(receptor site)或活性中心(active center)。
2. 受体的特性 受体具有下列特性。 (1) 特异性 受体对配体具有高度的识别能力,一种特定的受体只能与其特定的配体结合,产生特定的生理效应。同一化合物的不同光学异构体与受体的亲和力相差很大。 (2) 可逆性 受体与配体的结合是可逆的。受体与配体所形成的复合物可以解离,也可被另一种特异性配体所置换。 (3) 灵敏性 受体对配体具有高度的亲和力,微量的配体就能与受体结合而产生明显的效应。如5×10⁻¹⁸mol/L的乙酰胆碱溶液就能对蛙心产生明显的抑制作用。 (4) 饱和性 受体的数量有限,其能结合的配体量也是有限的,在药物的作用上表现为最大效应。当药物达到一定浓度后,其效应不会随其浓度的增加而继续增强。 (5) 多样性 同一受体可分布于不同的组织细胞,产生不同的效应;不同组织或同一组织的不同区域,受体密度不同。受体多样性是受体亚型分类的基础。
(二) 受体学说
为了阐明药物作用及其机制、药物分子结构与其药理效应之间的关系,自1913年Ehrlich提出“锁和钥”的假说作为配体-受体相互作用的模型以来,受体学说不断修改、补充和发展,择要简介如下。
1. 占领学说 该学说认为药物必须占领受体才能产生效应。效应的大小与药物占领的受体数量成正比,当受体全部被占领时,药物效应达到最大值。药物至少具备两种特性即亲和力和内在活性,才能产生生物效应,只有亲和力而没有内在活性的药物不能产生效应。
2. 速率学说 该学说认为药物作用主要取决于药物与受体结合和解离的速率,而与药物占领受体的数量无关。激动药结合和解离的速率均较快;部分激动药结合快,解离慢;拮抗药结合快,解离很慢。
3. 变构学说(二态学说) 该学说认为受体有两种可相互转化的构象状态,即活化状态(R*)和静息状态(R),激动药与R* 受体亲和力大,结合后产生效应并促使R向R* 转化;拮抗药与R受体亲和力大,结合后不产生效应并促进R* 向R转化,故能拮抗激动药的作用;部分激动药对两种状态的受体都有一定的亲和力,故有弱的效应。
(三) 受体的类型
根据受体的结构、位置及作用特点等,可将受体分为以下四种类型。
1. 离子通道受体 此类受体组成贯通细胞膜内外的离子通道。当受体激动时,离子通道开放,促进细胞内、外离子跨膜转运,使细胞膜去极化或超极化,引起兴奋或抑制效应。如N胆碱受体、GABA受体等。
2. G蛋白偶联受体 G蛋白是鸟苷酸结合调节蛋白的简称,存在于细胞膜内侧。G蛋白偶联受体是通过G蛋白连接细胞内效应系统的膜受体。其主要特点是,受体与激动剂结合后,经过G蛋白的转导而将信号传递至效应器引起药理效应。此类受体最多,如肾上腺素受体、多巴胺受体、前列腺素受体等。
3. 具有酪氨酸激酶活性的受体 这类受体镶嵌于细胞膜上,由三部分组成,细胞外段为配体结合区,中段穿透细胞膜,细胞内段具酪氨酸激酶活性,能激活细胞内蛋白激酶,增加DNA和RNA合成,加速蛋白质合成,从而产生细胞生长、分化等效应。如胰岛素受体、表皮生长因子受体等。
4. 调节基因表达的受体 又称细胞内受体。此类受体位于细胞内,其配体较易通过细胞膜的脂质双层结构,与细胞内的受体结合并发生反应,产生诱导蛋白质而呈现效应。如肾上腺皮质激素受体、甲状腺素受体等。
(四) 作用于受体的药物
药物与受体结合产生效应,必须具备两个条件,即亲和力(affinity)和内在活性(intrinsic activity)。亲和力是指药物与受体结合的能力,亲和力大结合强,亲和力小结合弱。亲和力大小常用亲和力指数pD₂表示,其值与亲和力成正比。内在活性是指药物与受体结合并激动受体产生最大效应的能力,也称效能(efficacy),用常数α表示。根据药物与受体结合后所产生的效应不同,可将作用于受体的药物分为三类。
1. 激动药(agonist) 也称为完全激动药(full agonist),是指与受体既有较强亲和力,又有较强内在活性(α=1)的药物,能与受体结合产生最大效应。如吗啡可激动阿片受体,产生强效镇痛作用。
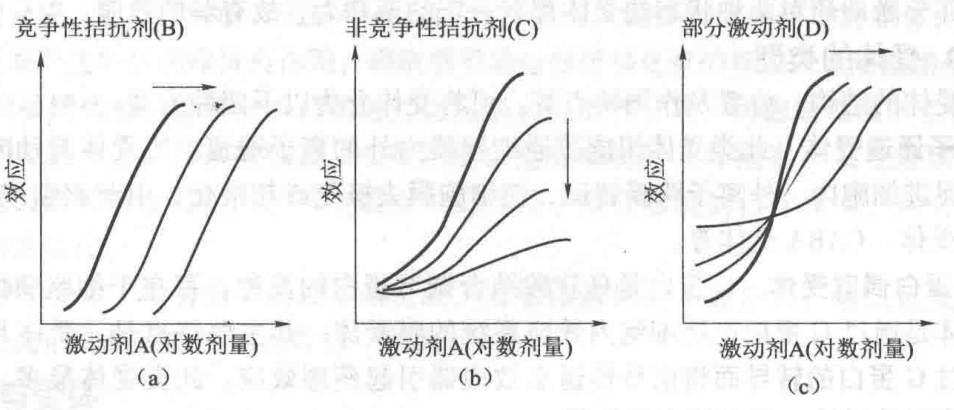
2. 拮抗药(antagonist) 是指与受体有较强亲和力,但无内在活性(α=0)的药物。此类药物本身不引起效应,但其占据受体后,可阻碍激动药与受体结合,对抗激动药的作用。如普萘洛尔与β受体结合,能阻断肾上腺素与β受体结合,呈现拮抗肾上腺素的作用,使心脏抑制。根据拮抗药与受体结合的性质不同,分为竞争性拮抗药和非竞争性拮抗药。 (1) 竞争性拮抗药(competitive antagonist) 可与激动药相互竞争与同一受体结合,产生竞争性抑制作用,可使激动药的量效曲线平行右移,但最大效应不变,见图1-1(a)所示。它说明,在竞争性拮抗药存在的情况下,可通过增加激动药剂量的方法使其效应恢复到原先单用激动药时的水平,即保持最大效应不变。 (2) 非竞争性拮抗药(non-competitive antagonist) 不与激动药竞争相同的受体,但它与受体结合(牢固或不可逆结合)后,可妨碍激动药与特异性受体结合,即使增加激动药的剂量,也不能达到单独应用激动药时的最大效应,亲和力和内在活性也均降低,不仅使激动药的量效曲线右移,也使最大效应降低,见图1-1(b)。
3. 部分激动药(partial agonist) 是指与受体有较强的亲和力,但仅有较弱的内在活性(α<1)的药物。其与受体结合后只能产生较弱的效应,即使浓度增加,也不能达到最大效应,却因占据受体而能拮抗激动药的部分效应,即表现为部分阻断作用。如喷他佐辛可产生较弱的镇痛效应,当其与吗啡合用时,可对抗后者镇痛作用的发挥,见图1-1(c)。
(五) 受体调节
受体调节(receptor regulation)是指受体的数量、亲和力和效应力在生理、病理和药理等因素的影响下而发生的变化,包括向上调节和向下调节。
1. 向上调节(up regulation) 是指受体数量增多,亲和力加大及效应力增强。向上调节的受体对药物非常敏感,可使药效增强,此现象称为受体超敏。受体超敏可因长期使用受体拮抗药而造成。如长期应用β受体拮抗药后,可使β受体向上调节,一旦突然停药,会出现反跳现象。
2. 向下调节(down regulation) 是指受体的数量减少、亲和力减弱及效应力降低。向下调节的受体对药物反应迟钝,药物效应减弱,此现象称为受体脱敏。受体脱敏可因多次使用受体激动药引起,是产生耐受性的原因之一。如长期应用β受体激动药异丙肾上腺素,可导致该药疗效逐渐变弱。
四、药物的构效关系与量效关系
(一) 药物的构效关系
构效关系(structure activity relationship)是指药物的化学结构与药理效应或毒性之间的关系。药物作用的性质取决于药物的化学结构,结构相似的药物可通过作用于同一靶点,引起相似或相反的效应。有些药物结构式相同,但光学活性不同而成为光学异构体(对映体),它们的药理效应不完全相同。如抗炎镇痛药萘普生,S-萘普生的抗炎作用是R-萘普生的28倍;氯霉素的左旋体有抗菌作用,右旋体无作用;左旋体的奎宁有抗疟作用,右旋体奎尼丁产生的却是抗心律失常作用。
了解药物的构效关系有助于深入认识药物的作用,对定向设计药物结构、研制开发新药等有重要的指导意义。如近年采用的计算机辅助药物设计,就是以药物构效关系原理为基础的。
(二) 药物的量效关系
药物剂量与效应关系(dose-effect relationship)简称量效关系。通过对量-效关系的分析,可了解药物剂量与产生相应效应之间的规律,为临床合理安全用药提供科学依据。
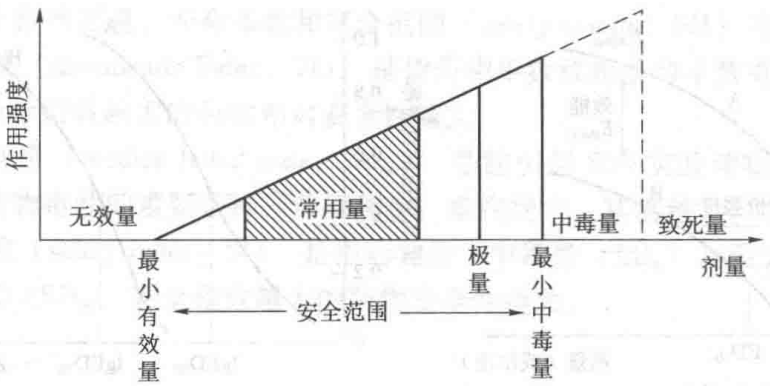
1. 药物剂量 药物剂量是指用药的分量,是决定血药浓度和药物效应的主要因素。在一定范围内,药物剂量的大小与血药浓度高低成正比,效应随着剂量的增加而增强。但若剂量过大,则可引起毒性反应,出现中毒甚至死亡,见图1-2。
(1) 无效量 不出现药理效应的剂量。 (2) 最小有效量(阈剂量) 能产生药理效应的最小剂量。 (3) 极量(最大治疗量) 是能产生最大治疗作用,但尚未引起毒性反应的剂量。极量是安全用药的极限。 (4) 治疗量和常用量 治疗量是最小有效量与极量之间的剂量。常用量是比最小有效量大,比极量小的剂量。常用量在一般情况下是安全而有效的剂量,药品说明书对药物的常用量都有明确规定。 (5) 最小中毒量 能引起毒性反应的最小剂量。 (6) 致死量 能引起机体中毒死亡的剂量。 (7) 安全范围 是最小有效量与最小中毒量之间的范围。安全范围越大,药物毒性越小,用药越安全。
2. 药物反应(效应) 药物的药理效应按所观察的指标不同,可分为量反应和质反应两种类型。 (1) 量反应 指药理效应的强弱可用连续增减的数量或最大效应的百分率表示,如心率、血压、尿量、血糖浓度、平滑肌收缩或松弛的程度等。其研究对象为单一的生物个体。 (2) 质反应 观察的药理效应只能用全或无、阳性或阴性表示,结果以反应的阳性率或阴性率作为统计量的反应类型,如死亡、惊厥、睡眠、麻醉等。研究对象为一个群体。
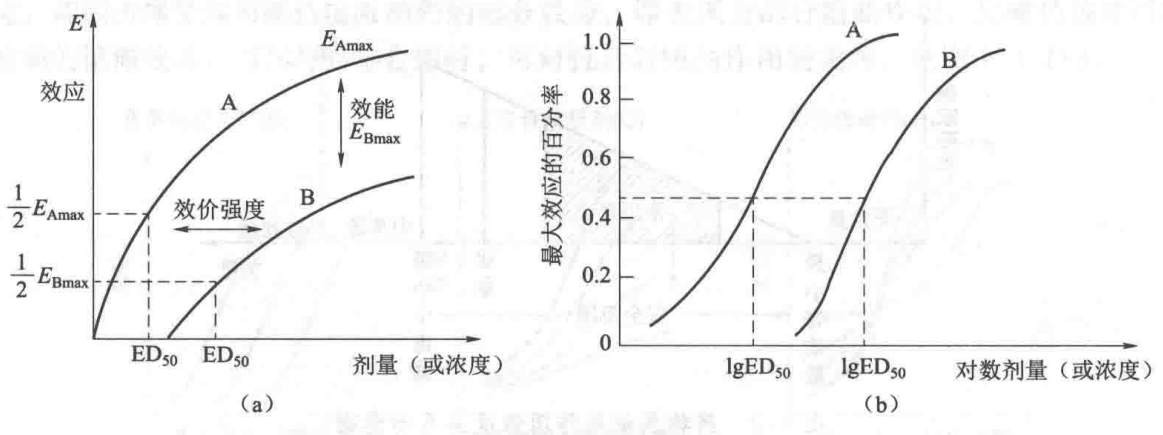
3. 量效曲线 量效曲线是以药物的效应为纵坐标,药物剂量或浓度(血药浓度)为横坐标,进行作图。 (1) 量反应量效曲线 量反应的量效曲线为一先陡后平的曲线,见图1-3(a)所示。为使量效规律更加直观,将横坐标的剂量转换成对数剂量,将效应转换成最大效应百分率,则量效曲线呈对称的S型曲线,见图1-3(b)所示。
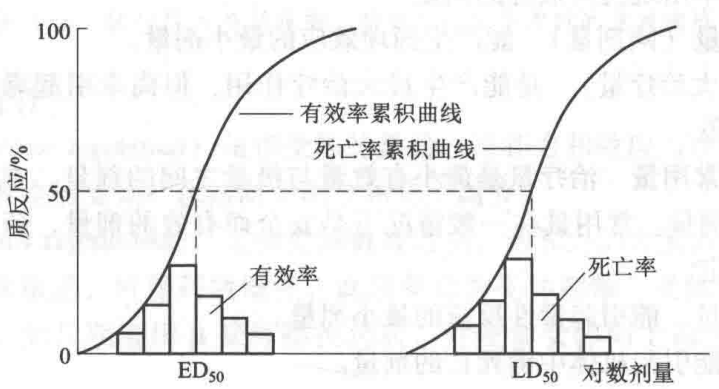
(2) 质反应量效曲线 质反应的量效曲线有两种状态,横坐标采用对数剂量,纵坐标采用反应频数时为常态分布曲线,说明大多数个体是在中等剂量时发生反应,少数是在较小剂量或很大剂量时才发生反应;若改用累加反应频数(发生反应的个数相加)为纵坐标,则为对称的S型曲线,见图1-4。
从量反应和质反应的两种量效曲线衍生出一些药理学基本概念,在临床中有重要意义。
斜率(slope) 在效应大约16%~84%区域,量效曲线几乎呈一直线,其与横坐标夹角的正切值为量效曲线的斜率。曲线的不同部位斜率不同,一般以中段最大。斜率大的药物剂量稍有增减,效应即有明显变化;反之亦然。斜率大小在一定程度上反映了临床用药剂量安全范围。
效能(efficacy) 指药物所能产生的最大效应(maximal effect, Eₘₐₓ),在质反应中阳性率达100%。效能反映了药物的内在活性,如吗啡类镇痛药效能高,能解除剧痛;阿司匹林类解热镇痛药效能低,只能用于轻、中度疼痛。
效价强度(potency) 指能引起等效反应的相对剂量或浓度,用于作用性质相同的药物之间等效剂量的比较。一般反映药物与受体的亲和力,其值越小,则强度越大。如图1-3(a)中,A、B两药的最大效应不同,Eₘₐₓ,A大于Eₘₐₓ,B;而在图1-3(b)中,A、B两药效能相同,而效价强度则是A药大于B药。
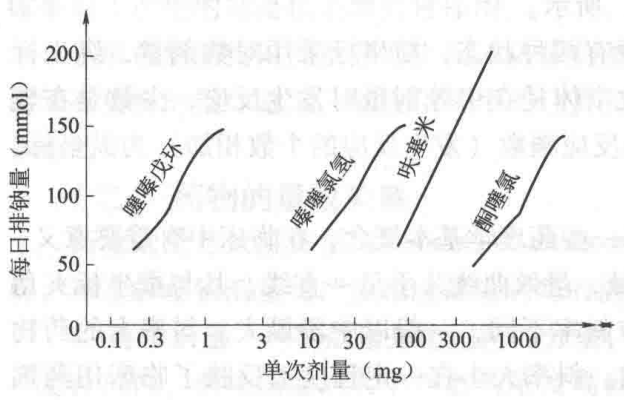
效能和效价强度反映药物的不同性质,二者具有不同的临床意义,常用于评价同类药物中不同品种的作用特点。例如利尿药以每日排钠量作为效应指标进行比较,氢氯噻嗪的利尿强度较呋塞米强;但以效能比较,则呋塞米较氢氯噻嗪强,见图1-5。因此,在比较两种或两种以上具有相同效应药物时,应从效能和效价强度两项指标综合考虑,单纯说某药比另一药物强是不适宜的。
图1-5 几种利尿药的效价强度和效能比较
半数有效量(median effective dose, ED₅₀) 是指能引起50%阳性反应(质反应)或50%最大效应(量反应)的剂量。半数有效量越小,表明药物活性(药理效应)越强;反之,药物活性越弱。
4. 药物的安全性评价 量效曲线还可用于分析药物的安全性。常用的安全性指标有治疗指数、半数致死量、安全指数和安全范围(safety margin, SM)等。 (1) 治疗指数(therapeutic index, TI) 是指药物半数致死量与半数有效量的比值,即TI=LD₅₀/ED₅₀。治疗指数越大的药物相对安全性越大。 (2) 半数致死量(median lethal dose, LD₅₀) 是能引起50%实验动物死亡的剂量。半数致死量是反映药物毒性的重要指标,其值越小,毒性越大,其值越大,毒性越小。 (3) 安全指数(safety index, SI) 是指药物最小中毒量(LD₁)与最大有效量(ED₉₉)的比值,即SI=LD₁/ED₉₉。安全指数越大的药物安全性越大。